Proteine in der Pole Position
Myxococcus xanthus ist ein räuberisches Bakterium der oberen Bodenschichten, das bei ausreichendem Nahrungsangebot in Kolonien, sogenannten Biofilmen, lebt. Innerhalb der Kolonie bewegen sich die einzelnen Zellen gleitend fort. Diese Art der Fortbewegung steht im Zentrum faszinierender sozialer Interaktionen: Schwarmbildung, Annäherung an Nahrung, oder auch, im Falle von Nahrungsmangel, der Bildung sporenhaltiger Fruchtkörper. Seine spezielle Lebensweise macht M. xanthus zu einem genialen Modellorganismus, um zu erforschen, wie sich Bakterien an wechselnde Umweltbedingungen anpassen. Doch wie funktioniert diese Fortbewegung auf molekularer Ebene?
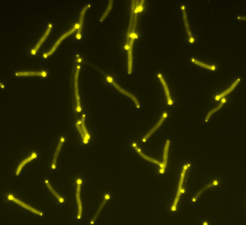
Die Arbeitsgruppe von Lotte Søgaard-Andersen am Max-Planck-Institut in Marburg möchte verstehen, wie M. xanthusauf Nahrungsmangel durch Bildung sporenhaltiger Fruchtkörper reagiert. Die Fähigkeit zur gleitenden Bewegung ist für M. xanthus zur Nahrungssuche und Fruchtkörperbildung essentiell. Die stäbchenförmigen Bakterien besitzen zwei Systeme zur Fortbewegung: ein Typ IV Pili-abhängiges System und ein System, das ihnen Gleitfähigkeit und damit auch unter wasserarmen Bedingungen Mobilität verleiht. Diese beiden Fortbewegungsmechanismen sind polar organisiert und bilden sich nur am vorderen Zellpol aus. Wenn M. xanthus die Bewegungsrichtung ändert, bauen sich die beiden Systeme ab und werden am neuen vorderen Zellpol wieder errichtet.
Dr. Dobromir Szadkowski aus der Søgaard-Andersen-Gruppe beschäftigt sich mit der Frage, wie die Lokalisation und der Aufbau der Fortbewegungssysteme am vorderen Zellpol ablaufen. „Zu Beginn unserer Forschungen wussten wir, dass mindestens drei Proteine an dieser Regulation beteiligt sein mussten. MgIA ist eine kleine Ras-ähnliche GTPase, die in ihrer GTP-gebundenen Form die Bewegung auslöst. Das zweite, MgIB, ist ein GTPase-aktivierendes Protein (GAP). Auch war bekannt, dass das Protein RomR wichtig für die polare Lokalisation von MgIA-GTP ist. MgIA-GTP ist am vorderen Zellpol lokalisiert, MglB und RomR hingegen sind asymmetrisch an beiden Zellpolen lokalisiert, finden sich aber vor allem am hinteren Zellpol, “ erklärt Dr. Szadkowski.
Ausgangspunkt dieser neuen Arbeiten war die Beobachtung, dass kleine GTPasen in Eukaryonten nicht nur auf ein GAP zur effizienten GTP Hydrolyzse angewiesen sind, sondern auch auf einen Guanin Nucleotide Austauschfaktor (GEF), der GDP effizient in GTP umwandelt. Dr. Szadkowski ergänzt: “Wir machten uns auf die Suche nach einem GEF für MglA, und fanden ein Protein, dass wir nun als RomX bezeichnen.“ Wie erwartet, ist RomX für die Gleitfähigkeit essentiell. Auch fanden die Forscher, dass RomX in den Zellpolen lokalisiert ist und diese Lokalisation wiederum von der RomR-Aktivität abhängt. Und mehr als das: der RomR/RomX Komplex besitzt GEF Aktivität und steuert die polare Lokalisation von MgIA-GTP.
Aus der Summe dieser Ergebnisse postulierten die Forscher folgenden Ablauf: In der M. xanthus Zelle leitet RomR das RomX zu den Zellpolen. Der Komplex aus beiden Proteinen wiederum leitet MgIA-GTP auf zweierlei Weise zum vorderen Zellpol: zunächst stimuliert RomR/RomX durch seine GEF-Aktivität die Akkumulation von MgIA; des Weiteren bindet der Komplex MgIA-GTP am vorderen Zellpol.
Beide Aktivitäten führen zu einer Anreicherung von MgIA-GTP an diesem Pol und lösen die Bewegung aus. MgIA wird vom hinteren Zellpol ferngehalten, weil dort MgIB mit seiner GAP Aktivität lokalisiert ist. Dadurch stellen die räumlich getrennten Aktivitäten des RomR/RomX-Komplexes und des MgIB GAP die polare Ausrichtung sicher. Der RomR/RomX Komplex ist der erste bakteriellen Nukleotid-Austauschfaktor, der im Zusammenhang mit bakterieller Polarität gefunden wurde.
Interessanterweise zeigen die Kontroll-Faktoren GEF und GAP des Proteins MglA eine räumliche Verteilung innerhalb der Zelle, die der Organisation der Faktoren der kleinen GTPasen von Eukaryonten, wie sie im Zusammenhang mit Zellpolarität und Zellbewegung steht, überraschend ähnelt. Während jedoch MgIA bei Prokaryonten häufig vorkommt, sind RomR und RomX sehr viel seltener zu finden. Das deutet darauf hin, dass hier vermutlich weitere GEF an der Regulation MgIA-ähnlicher Proteinen beteiligt sind.
Diese Arbeit wurde finanziell unterstützt von der Deutschen Forschungsgemeinschaft (DFG) im Rahmen des Sonderforschungsbereiches Transregio 174 „Räumliche-zeitliche Dynamik bakterieller Zellen“ sowie der Max-Planck-Gesellschaft.










