Schutz der [Fe]-Hydrogenase
Hydrogenase-Enzyme katalysieren die Produktion und Nutzung von Wasserstoffgas, welches als zukünftiger Energieträger gilt. Wissenschaftler vom Max-Planck-Institut für terrestrische Mikrobiologie in Marburg entdeckten in Kooperation mit dem Max-Planck-Institut für Biophysik, das die [Fe]-Hydrogenase durch Konformationsänderungen des Proteins geschützt wird. Diese Erkenntnis ist entscheidend für die zukünftige Anwendung von Hydrogenasen und das Verständnis des katalytischen Mechanismus dieses Enzyms.
[Fe]-Hydrogenase vermittelt den reversiblen Hydridtransfer von H2 auf eine organische Verbindung. Diese katalytische Fähigkeit macht [Fe]-Hydrogenase zu einem attraktiven Modellsystem für das Design mimetischer Hydrierungskatalysatoren. Bis heute wurden bereits zahlreiche mimetische Verbindungen des aktiven Zentrums der [Fe]-Hydrogenase synthetisiert. Ein Merkmal und damit auch ein potentielles Problem bei der Anwendung der [Fe]-Hydrogenase ist die Licht- und Luftempfindlichkeit ihres mimetischen Katalysators. Dies macht die Entwicklung einer Strategie zum Schutz der [Fe]-Hydrogenase notwendig.
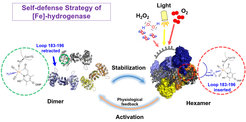
In der hexameren Ruheform (rechts) ist das Eisenzentrum durch Bindung von Asp 189 aus dem Oligomerisierungsloop eines Nachbardimers an das Eisenzentrum vor Licht, O2 und H2O2 geschützt. Durch eine hohe Konzentration der Substrate wird die aktive dimere Form gefördert indem die Oligomerisierungsschleife freigesetzt wird (links).
Der Schutz von Metalloenzymen vor Umwelteinflüssen ist ein lebenswichtiger Prozess für das Überleben von Mikroorganismen in natürlichen Lebensräumen. Dies hat die Natur dazu gezwungen erstaunlich kreative Lösungen zu entwickeln, um ihre Enzyme aktiv zu halten. Die Arbeitsgruppe von Seigo Shima am Max-Planck-Institut für terrestrische Mikrobiologie in Marburg hat gemeinsam mit Ulrich Ermler vom Max-Planck-Institut für Biophysik einen Schutzmechanismus in der Kristallstruktur der nativen [Fe]-Hydrogenase aus Methanothermobacter marburgensis gefunden. Basierend auf Strukturdaten und der biochemischen Analyse fanden die Wissenschaftler heraus wie [Fe]-Hydrogenase auf natürliche Weise stabilisiert und vor Licht und oxidativem Stress geschützt wird. Das Enzym ist als Dimer aktiv, jedoch licht- und luftempfindlich. Dahingegen ist das Enzym in der Ruheform als Hexamer inaktiv, das Eisen des Cofaktors mit aktivem Zentrum hingegen wird durch Bindung an einen Aspartatrest geschützt, der aus einem Loop eines anderen Dimers des Hexamers hervorspringt (Abbildung 1). Dieses Zusammenspiel zwischen Aktivität und Stabilität durch dynamische Dimer-Hexamer-Transformationen und Ligandenaustausch stellt eine neue Art des Schutzes dar. Dieser Schutzmechanismus kann als Inspiration für die Entwicklung robuster Hydrogenase und Mimetika dienen.










