Auf Effizienz gepolt: Wie methanogene Mikroben Elektronen steuern
Ein gigantischer Enzymkomplex ermöglicht es methanogenen Mikroorganismen, unter extrem energiearmen Lebensbedingungen zu gedeihen
Methanogene Archaeen nutzen ausgeklügelte Mechanismen, um in energiearmen und sauerstofffreien Umgebungen zu leben. Ein Schlüsselmechanismus zur Einsparung von Energie ist die sogenannte Elektronenbifurkation, eine Reaktion, bei der die Energie eines Elektronenpaares "aufgespalten" wird, sodass ein Elektron auf Kosten des anderen energiereicher wird. Forschende der Max-Planck-Institute für terrestrische Mikrobiologie (Marburg) und Biophysik (Frankfurt am Main) haben einen gigantischen Enzymkomplex aus einem methanogenen Archaeon entdeckt, der Elektronen aus der Elektronenbifurkation direkt an CO2-Reduktion und -Fixierung überträgt. Ihre detaillierten Einblicke in diese effizienten Energieumwandlungsprozesse können neue Möglichkeiten für nachhaltige biotechnologische Entwicklungen eröffnen.
Schätzungsweise eine Milliarde Tonnen Methan werden jährlich von anaeroben Mikroorganismen, sogenannten methanogenen Archaeen, produziert. Da Methan ein starkes Treibhausgas ist, bedrohen steigende atmosphärische Methankonzentrationen das Leben und die Lebensgrundlagen auf unserer Erde. Andererseits kann durch anaerobe Vergärung von Abfällen und Abwässern gewonnenes Methan als erneuerbare Brennstoffquelle dienen. Ein besseres Verständnis der Mechanismen der mikrobiellen Methanbildung birgt daher das Potenzial, Maßnahmen zur Erhaltung einer intakten Umwelt zu fördern und umzusetzen.
Methanogene Archaeen konkurrieren erfolgreich mit anderen Mikroorganismen, indem sie Methanogenese durchführen, einen der letzten Schritte im anaeroben Abbau organischer Nährstoffe - oft unter extremen Bedingungen. Die meisten methanogenen Archaeen produzieren Methan aus Kohlenstoffdioxid (CO2) und gasförmigem Wasserstoff (H2) über den methanogenen Zyklus, der mehrere Enzymreaktionen umfasst. In typischen Lebensräumen methanogener Mikroben wird bei dieser Reaktion nur eine geringe Menge an Energie freigesetzt, sodass sie hocheffiziente Enzymsysteme benötigen, um in solchen energiearmen Umgebungen zu gedeihen.
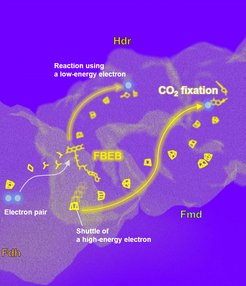
Ein besonders ausgeklügelter Schritt des methanogenen Zyklus ist die sogenannte flavinbasierte Elektronenbifurkation (FBEB). Bei dieser Reaktion wird die Energie eines Elektronenpaares geteilt, sodass ein Elektron auf Kosten des anderen stärker reduzierend wirkt. Bisher wurde angenommen, dass Methanogene das energiereiche Elektron über Ferredoxin übertragen, einem kleineren frei in der Zelle diffundierenden Protein.
Nun hat ein Forscherteam am MPI für terrestrische Mikrobiologie (Marburg) und am MPI für Biophysik (Frankfurt) überraschenderweise gezeigt, dass ein solcher Elektronenträger für den Elektronentransfer von FBEB zur CO2-Reduktion nicht notwendig ist. Die Forschenden reinigten zunächst Enzymkomplexe bestehend aus Formiat-Dehydrogenase (Fdh), Heterodisulfidreduktase (Hdr) und Formylmethanofuran-Dehydrogenase (Fmd) aus dem methanogenen Archaeon Methanospirillum hungatei. Diese Spezies ist, wie viele andere Methanogene, häufig in anaeroben Fermentern zu finden, die organische Reste aus häuslichen Abwässern oder industriellen Abfällen aufbereiten.
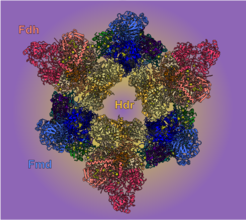
Die Aufklärung der Strukturen mittels kryogener Elektronenmikroskopie (Kryo-EM) zeigte, dass die Enzyme, die den letzten und den ersten Schritt des methanogenen Zyklus katalysieren, einen gigantischen Komplex bilden. Dieser verbindet diese beiden Schritte, die formatgetriebene FBEB und die CO2-Reduktion, direkt miteinander, ohne dabei den Elektronenträger Ferredoxin zu verwenden.
"Unsere Strukturanalyse zeigte uns einen riesigen Enzymkomplex", sagt Tomohiro Watanabe, Hauptautor der Studie. "Ein Elektronenübertragungsprotein, Polyferredoxin, bildet einen leitenden Pfad, der die energiereichen Elektronen von FBEB direkt zur CO2-Reduktion führt statt über einen löslichen Träger. Das bedeutet weniger Gefahr, wertvolle Elektronen zu verlieren."
Strukturvergleiche sowie bekannte Interaktionstests legen nahe, dass solche übergeordneten Strukturen der Hdr- und Fmd-Komplexe in diversen methanogenen Archaeen vorkommen könnten.Die Strukturen geben auch neue Einblicke in den fein abgestimmten Mechanismus von FBEB. Forschungsgruppenleiterin Bonnie Murphy erklärt: "Die Methode der Kryo-EM ermöglicht es uns, über Bildklassifizierung Strukturen verschiedener Konformationszustände zu lösen, die aus derselben Probe stammen. In diesem Fall fanden wir einen „mobilen Arm“, der zwischen zwei verschiedenen Konformationszuständen rotiert. Dadurch steuert der Komplex den Elektronenfluss zu und aus dem FBEB-Zentrum."
Insgesamt helfen diese Erkenntnisse zu verstehen, wie der Energiestoffwechsel methanogener Mikroben auf Effizienz getrimmt ist. Dieses Wissen wird bei der Entwicklung von Strategien zur Verringerung von Treibhausgasemissionen hilfreich sein und könnte eine breitere Anwendung der Elektronenbifurkation in der Biotechnologie ermöglichen.













