Ein neues Puzzleteil im globalen Kohlenstoffzyklus
Forschungsbericht (importiert) 2019 - Max-Planck-Institut für terrestrische Mikrobiologie
Einleitung
Von Charles Darwin ist überliefert, dass er im „klaren blauen Wasser“ des Ozeans etwas vermutete, das noch kleiner sei als die Protozoen, die er im Mikroskop erkennen konnte. Heute wissen wir, dass jeder Liter Ozeanwasser von Hunderten von Millionen Mikroorganismen wimmelt. Obwohl sie selbst nur Mikrometer klein sind, bestimmen sie durch ihre schiere Anzahl und ihre hohe Stoffwechselrate maßgeblich den Energiefluss und den Umsatz von Biomasse in den Weltmeeren (Abb. 1).

Abb. 1: Auf Satellitenbildern wirken die Algenteppiche mit ihren hellen Schlieren wie Kunstwerke. Allein in der etwa 70.000 Quadratkilometer umfassenden Deutschen Bucht entstehen bei der Algenblüte im Frühjahr etwa zehn Millionen Tonnen Biomasse.
Während einzellige Algen, auch bekannt als Phytoplankton, Kohlendioxid in Biomasse umwandeln, kommen andere Mikroorganismen vor allem dann zum Zuge, wenn die Algen den fixierten Kohlenstoff ausscheiden oder – manchmal schlagartig, wie nach der sogenannten Algenblüte – absterben. Noch im Oberflächenwasser verarbeiten die Einzeller viele Tausend Tonnen der Algen-Biomasse: ein zentraler Prozess im marinen Lebenszyklus. Eine der wichtigsten Verbindungen im Ozean ist dabei die Glycolsäure, ein direktes Nebenprodukt der Fotosynthese. Diese wird von marinen Bakterien teilweise wieder in Kohlendioxid zurück verwandelt. Doch das genaue Schicksal des Kohlenstoffs in der Glycolsäure war bislang nicht bekannt. Um die Lokalisierung, Raten und Umsätze der Nährstoffnetze im Ozean zu verstehen, ist eine genauere Kenntnis des bakteriellen Abbaus der Algen-Biomasse vonnöten. Was geschieht also mit dem Kohlenstoff der Glycolsäure, bei dem es global immerhin um Stoffmengen im Bereich von einer Milliarde Tonnen pro Jahr geht?
Der vergessene Stoffwechselweg
Nicht immer müssen Forscherinnen und Forscher ganz von vorne beginnen. Manchmal gibt es bereits bekannte Puzzleteile, sie müssen nur erkannt und an die richtige Stelle gelegt werden. Ein solches Teil ist der β-Hydroxyaspartat-Zyklus (BHA-Zyklus), der vor mehr als 50 Jahren in dem Bodenbakterium Paracoccus entdeckt wurde (Abb. 2; [1]). Damals erfuhr der Stoffwechselweg wenig Aufmerksamkeit, seine genauen biochemischen Abläufe blieben unerforscht. Als wir im Rahmen von Literaturrecherchen auf diesen Stoffwechselweg stießen, fiel uns auf, dass er effizienter sein müsste als der bisher für den Abbau der Glycolsäure angenommene Prozess. Könnte dieser Stoffwechselweg nicht vielleicht mehr Bedeutung besitzen als ursprünglich angenommen?
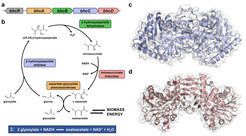
Ausgestattet mit einer einzelnen Gensequenz stießen wir in Datenbanken auf ein Cluster aus insgesamt vier Genen, die die Bauanleitung für vier Enzyme liefern. In Kombination miteinander waren drei der Enzyme ausreichend, um eine aus der Glycolsäure abgeleitete Verbindung weiter umzusetzen. Doch wofür war das vierte Enzym zuständig? Als wir dieses Enzym im Labor testeten, entdeckten wir, dass es eine bisher unbekannte Reaktion katalysiert, eine sogenannte Iminreduktion. Durch diese vierte Reaktion schließt sich der Stoffwechselweg zu einem eleganten Kreislauf, durch den der Kohlenstoff der Glycolsäure ohne Verlust von CO2 zirkuliert werden kann [2]. In unserer Studie beschreiben wir die vollständige Reaktionssequenz des BHA-Zyklus und die Kristallstrukturen seiner beiden Schlüsselenzyme, darunter ein völlig neues Enzym, die Iminosuccinatreduktase, die der Ausgangspunkt einer neuen Familie von primären Iminreduktasen ist.
Weltweit verbreitet, ökologisch bedeutsam
In Zusammenarbeit mit Wissenschaftlern der Universität Marburg gelang es uns, den Glycolsäure-Stoffwechsel und seine Regulation in den lebenden Mikroorganismen zu studieren. Nun ging es darum, das Vorkommen und die Aktivität dieser Gene im marinen Lebensraum und ihre ökologische Bedeutung nachzuweisen. Hierfür erwies sich eine Zusammenarbeit mit den Meeresforscherinnen und – forschern des Bremer Max-Planck-Instituts als besonders fruchtbar, denn diese untersuchen bereits seit Jahren die marinen Lebensgemeinschaften bei Helgoland, insbesondere die Bakterienpopulationen während und nach Algenblüten. In mehreren Exkursionen auf hoher See maßen wir die Bildung und den Verbrauch von Glycolsäure während der Algenblüte im Frühjahr 2018. Und tatsächlich: Der BHA-Zyklus war aktiv am Stoffwechsel der Glycolsäure beteiligt.
Auch in den bakteriellen Genomsequenzen, welche die TARA Oceans-Expedition auf den Weltmeeren sammelte, fanden sich immer wieder die Baupläne des Stoffwechselzyklus, und zwar im Durchschnitt 20mal häufiger als alle anderen postulierten Abbaurouten für Glycolsäure. Der wiederentdeckte Stoffwechselweg fristet also kein Nischendasein, sondern ist im Gegenteil weit verbreitet. Das stellt unser bisheriges Verständnis zum Schicksal der Glycolsäure auf den Kopf. Die Daten zeigen, dass wir den Kreislauf von Milliarden Tonnen Kohlenstoff in den Weltmeeren neu bewerten müssen. Diese Arbeit macht uns außerdem bewusst, welche globalen Ausmaße der Stoffwechsel von Mikroorganismen annehmen kann.

